आवर्त सारणी रसायन विज्ञान की एक महत्वपूर्ण और बुनियादी उपकरण है जो सभी ज्ञात तत्वों को उनके परमाणु संख्या, गुणधर्म और रासायनिक व्यवहार के आधार पर व्यवस्थित करती है। यह सारणी, जिसे पहले पहल 1869 में रूसी वैज्ञानिक दिमित्री मेंडेलीव द्वारा प्रस्तुत किया गया था, तत्वों के बीच संबंधों को समझने में एक क्रांतिकारी भूमिका निभाती है। आवर्त सारणी न केवल तत्वों को समूहों और आवर्तों में वर्गीकृत करती है, बल्कि यह तत्वों के विभिन्न भौतिक और रासायनिक गुणों की भविष्यवाणी करने में भी मदद करती है। इस लेख में, हम आवर्त सारणी की संरचना, तत्वों के समूह, उनकी विशेषताएँ और इसके नियमों पर विस्तृत चर्चा करेंगे, जिससे रसायन विज्ञान के इस महत्वपूर्ण उपकरण की व्यापक समझ प्राप्त हो सके।
तत्वों के वर्गीकरण का इतिहास
तत्वों के वर्गीकरण का इतिहास विज्ञान में एक महत्वपूर्ण अध्याय है, जिसने रसायन विज्ञान की नींव को मजबूत किया। विभिन्न वैज्ञानिकों ने समय-समय पर तत्वों को वर्गीकृत करने के लिए कई प्रयास किए, जिनमें से कुछ प्रमुख प्रयास निम्नलिखित हैं:
लेवॉयसियर का वर्गीकरण (1789)
एंटोनी लेवॉयसियर ने तत्वों को धातुओं और अधातुओं में वर्गीकृत किया। उन्होंने 33 तत्वों की एक सूची बनाई और उन्हें चार समूहों में विभाजित किया: गैस, धातु, अधातु और मृत्तिका (earths)।
डोबेराइनर की त्रिक (1829)
जोहान डोबेराइनर ने तत्वों को त्रिकों में वर्गीकृत किया। उन्होंने पाया कि कुछ तत्वों के समूहों में, मध्य तत्व का परमाणु भार अन्य दो तत्वों के औसत के बराबर होता है। उदाहरण के लिए, कैल्शियम (Ca), स्ट्रोंटियम (Sr), और बेरियम (Ba)।
न्यूलैंड्स का अष्टक नियम (1864)
जॉन न्यूलैंड्स ने तत्वों को उनके बढ़ते परमाणु भार के आधार पर व्यवस्थित किया और पाया कि हर आठवें तत्व का गुणधर्म पहले तत्व के समान होता है। इसे उन्होंने अष्टक नियम (Law of Octaves) कहा। हालांकि, यह नियम उच्च तत्वों के लिए उपयुक्त नहीं था।
मेंडेलीव की आवर्त सारणी (1869)
दिमित्री मेंडेलीव ने तत्वों को उनके बढ़ते परमाणु भार के आधार पर व्यवस्थित किया और आवर्त सारणी का निर्माण किया। मेंडेलीव की सारणी में तत्वों के गुणधर्मों में आवर्तिता देखी गई। उन्होंने कुछ खाली स्थान भी छोड़े और भविष्यवाणी की कि इन स्थानों को भविष्य में खोजे जाने वाले तत्व भरेंगे।
मोस्ले का परमाणु संख्या पर आधारित वर्गीकरण (1913)
हेनरी मोस्ले ने तत्वों को उनके परमाणु संख्या के आधार पर पुनर्व्यवस्थित किया। उन्होंने यह सिद्ध किया कि तत्वों के गुणधर्म उनके परमाणु संख्या पर निर्भर करते हैं न कि उनके परमाणु भार पर। इसके बाद आधुनिक आवर्त सारणी का निर्माण हुआ।
आवर्त सारणी (Periodic Table)
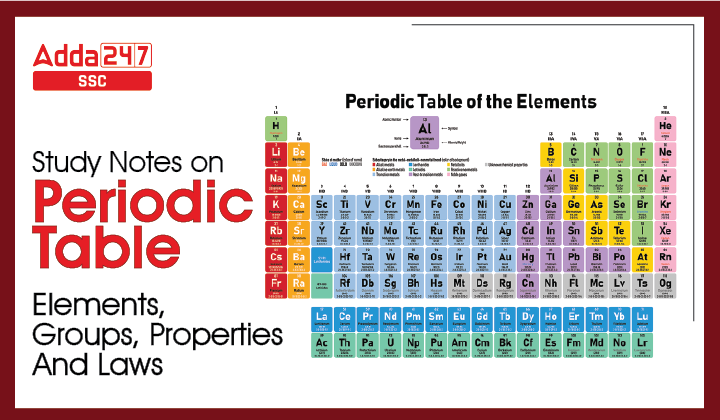
आवर्त सारणी एक संरचित प्रतिनिधित्व का कार्य करती है, तत्वों को उनकी विशिष्ट रासायनिक विशेषताओं के आधार पर व्यवस्थित करने के रूप में। आधुनिक रूप में, इसमें 18 समूह और 7 कालानुक्रम होते हैं। परमाणु संख्या के आधार पर परमाणुओं की व्यवस्था की प्रगति को दिमित्री मेंडेलीव ने प्रारंभ किया था। यहां, हमने आवर्त सारणी के समूहों से संबंधित महत्वपूर्ण जानकारी प्रस्तुत की है, जो परीक्षा की तैयारी के लिए बहुत फायदेमंद हो सकती है।

आवर्त सारणी के तत्वों की सूची
118 तत्वों को 7 आवर्त और 18 समूहों में व्यवस्थित किया गया है जैसा कि ऊपर दिखाया गया है। इसके अलावा, तत्वों को विभिन्न ब्लॉकों में विभाजित किया गया है।
समूह 1 (क्षार धातु अर्थात् एल्किन)
विशेषता:
• क्षार धातुएं चांदी के रंग (सीज़ियम का रंग सुनहरा होता है), नरम, कम घनत्व वाली धातुएं होती हैं।
• इन सभी तत्वों की संयोजकता एक इलेक्ट्रॉन की होती है जो आसानी से खो जाता है और एक धनात्मक आवेश वाला आयन बनता है।
• उनकी आयनीकरण ऊर्जा सबसे कम होती है। यह उन्हें बहुत क्रियाशील बनाता है और वे काफी सक्रिय धातु हैं।
• उनकी क्रियाशीलता के कारण, वे स्वाभाविक रूप से आयनिक यौगिक होते हैं, न कि मौलिक अवस्था में।
• क्षार धातुएं हैलोजन के साथ आसानी से प्रतिक्रिया करके आयनिक लवण बनाती हैं, जैसे सोडियम क्लोराइड (NaCl)।
• वे जल के साथ अभिक्रिया करके हाइड्रोजन गैस मुक्त करते हैं।
Alkali metal + water → Alkali metal hydroxide + hydrogen
समूह 2 क्षारीय पार्थिव धातु
आवर्त सारणी के समूह 2 श्रृंखला में बेरिलियम (Be), मैग्नीशियम (Mg), कैल्शियम (Ca), स्ट्रोंटियम (Sr), बेरियम (Ba) और रेडियम (Ra) तत्व शामिल हैं।
आवर्त सारणी तत्वों के समूह 2 की विशेषता
• क्षारीय पार्थिव धातु चांदी के रंग की, मुलायम, कम घनत्व वाली धातुएं होती हैं, हालांकि ये क्षार धातुओं की तुलना में थोड़ी सख्त होती हैं।
• इन सभी तत्वों की संयोजकता दो इलेक्ट्रॉन की होती हैं और दोनों को खोने की प्रवृत्ति दो-प्लस आवेश के साथ आयन बनाने के लिए होती है।
•बेरिलियम इस समूह का सबसे कम धात्विक तत्व है और इसके यौगिकों में सहसंयोजक बंध बनाने की प्रवृत्ति होती है।
• वे हैलोजन के साथ आसानी से अभिक्रिया करके आयनिक लवण बनाते हैं और पानी के साथ धीरे-धीरे अभिक्रिया कर सकते हैं।
समूह 13 (बोरॉन समूह)
आवर्त सारणी के समूह 13 में बोरॉन (B), एल्युमिनियम (Al), गैलियम (Ga), इंडियम (In), थैलियम (Tl) तत्व शामिल हैं।
आवर्त सारणी तत्वों के समूह 13 की विशेषता
• इस समूह में, हम अधात्विक प्रकृति की ओर परिवर्तन देखते हैं। बोरॉन एक उपधातु है, इसमें धातुओं और गैर-धातुओं के बीच की विशेषताएं हैं, और बाकी समूह धातु हैं।
• इन तत्वों की संयोजकता तीन इलेक्ट्रॉन की होती हैं। आयनिक यौगिकों में तीन-प्लस चार्ज के साथ आयन बनाने के लिए धातुएं तीनों इलेक्ट्रॉनों को खो सकती हैं।
• एल्युमिनियम पृथ्वी की परत में तीसरा सबसे प्रचुर तत्व(7.4 प्रतिशत) है, और इसका व्यापक रूप से पैकेजिंग सामग्री में उपयोग किया जाता है। एल्युमिनियम एक सक्रिय धातु है, लेकिन स्थिर ऑक्साइड धातु पर एक सुरक्षात्मक कोटिंग बनाता है जो इसे जंग के लिए प्रतिरोधी बनाता है।
समूह 14 (कार्बन समूह)
आवर्त सारणी के समूह 14 में कार्बन (C), सिलिकॉन (Si), जर्मेनियम (Ge), टिन (Sn), और लेड (Pb) तत्व शामिल हैं।
आवर्त सारणी के समूह 14 के तत्व की विशेषता
• इस समूह में अधातु कार्बन, दो उपधातु और दो धातुओं के साथ मिश्रित प्रकार का तत्व है। इसकी सामान्य विशेषता चार इलेक्ट्रॉन की हैं।
• दो धातुएं, टिन और सीसा, अप्रतिक्रियाशील धातु हैं और दोनों आयनिक यौगिकों में दो-प्लस या चार-प्लस चार्ज के साथ आयन बना सकते हैं।
• कार्बन मोनोआटोमिक आयनों के बजाय यौगिकों में चार सहसंयोजक बंध बनाता है। तात्विक अवस्था में, इसके कई रूप हैं, जिनमें से सबसे प्रसिद्ध ग्रेफाइट और हीरा हैं।
• सिलिकॉन कुछ मामलों में कार्बन के समान होता है, यह चार सहसंयोजक बंध बनाता है, लेकिन यह यौगिकों की एक विस्तृत श्रृंखला नहीं बनाता है। सिलिकॉन पृथ्वी की परत(25.7 प्रतिशत) में दूसरा सबसे प्रचुर तत्व है और हम सिलिकॉन युक्त सामग्री ईंटें, मिट्टी के बर्तन, चीनी मिट्टी के बरतन, स्नेहक, सीलेंट, कंप्यूटर चिप्स और सौर सेल से घिरे हुए हैं।
• सबसे सरल ऑक्साइड, सिलिकॉन डाइऑक्साइड (SiO2) या सिलिका, कई चट्टानों और खनिजों का एक घटक है।
समूह 15 (नाइट्रोजन समूह)
नाइट्रोजन समूह आवर्त सारणी के समूह 15 (पूर्व में समूह V) में तत्वों की श्रृंखला है। इसमें नाइट्रोजन (N), फास्फोरस (P), आर्सेनिक (As), सुरमा (Sb), और बिस्मथ (Bi) तत्व शामिल हैं। इस समूह के तत्वों के लिए सामूहिक नाम pnictogens भी कभी-कभी उपयोग किया जाता है।
आवर्त सारणी के समूह 15 के तत्व की विशेषता
• इन सभी तत्वों की संयोजकता पांच इलेक्ट्रॉन की होती हैं। नाइट्रोजन और फास्फोरस अधातु हैं। वे नाइट्राइड और फॉस्फाइड आयनों के साथ काफी अस्थिर आयन बनाने के लिए तीन इलेक्ट्रॉन प्राप्त कर सकते हैं।
• नाइट्रोजन, एक द्विपरमाणुक अणु के रूप में वायु का प्रमुख घटक है और दोनों तत्व जीवन के लिए आवश्यक हैं। मानव शरीर में नाइट्रोजन वजन का लगभग 3 प्रतिशत और फॉस्फोरस लगभग 1.2 प्रतिशत होता है। व्यावसायिक रूप से, ये तत्व उर्वरकों के लिए महत्वपूर्ण हैं। आर्सेनिक और एंटीमनी उपधातु हैं, और बिस्मथ समूह में एकमात्र धातु है। तीन-प्लस चार्ज के साथ आयन बनाने के लिए बिस्मथ तीन इलेक्ट्रॉनों को खो सकता है।
•बिस्मथ भी पूरी तरह से स्थिर तत्व है जो रेडियोधर्मी रूप से अन्य सरल तत्वों का क्षय नहीं करता है।
समूह 16 (Chalcogens)
वे ऑक्सीजन (O), सल्फर (S), सेलेनियम (Se), टेल्यूरियम (Te), रेडियोधर्मी पोलोनियम (Po), और सिंथेटिक अनहेक्सियम (Uuh) हैं।
आवर्त सारणी के समूह 16 के तत्व की विशेषता:
• इस समूह की संयोजकता छह इलेक्ट्रॉन की हैं। ऑक्सीजन और सल्फर अधातु हैं; उनका मौलिक रूप आणविक है, और वे दो इलेक्ट्रॉनों को प्राप्त कर सकते हैं और दो ऋणात्मक आवेश के साथ आयन बना सकते हैं।
•सल्फर में संभवत: किसी भी तत्व की तुलना में सबसे अधिक अपररूप होते हैं, हालांकि सबसे सामान्य और स्थिर रूप S8 अणुओं के पीले क्रिस्टल हैं।
समूह 17 (हैलोजन)
हैलोजन आवर्त सारणी के समूह 17 (पूर्व में समूह VII या VIIa) के तत्व हैं। वे फ्लोरीन (F), क्लोरीन (Cl), ब्रोमीन (Br), आयोडीन (I), एस्टैटिन (At) हैं।
आवर्त सारणी के समूह 17 के तत्व की विशेषता:
• इन सभी तत्वों की संयोजकता सात इलेक्ट्रॉन की होती हैं।
• यह समूह पूरी तरह से अधातुओं से युक्त पहला समूह है।
• वे अपनी प्राकृतिक अवस्था में द्विपरमाणुक अणुओं के रूप में मौजूद रहते हैं।
• कमरे के तापमान पर, फ्लोरीन और क्लोरीन गैसों के रूप में, ब्रोमीन एक तरल के रूप में, और आयोडीन एक ठोस के रूप में मौजूद होते हैं।
• उन्हें अपने बाहरी इलेक्ट्रॉन कक्षों को भरने के लिए एक और इलेक्ट्रॉन की आवश्यकता होती है, और इसलिए एकल-आवेशित नकारात्मक आयन बनाने के लिए एक इलेक्ट्रॉन प्राप्त करने की प्रवृत्ति होती है। इन ऋणात्मक आयनों को हैलाइड आयन कहा जाता है, और इन आयनों वाले को हैलाइड कहा जाता है।
• हैलोजन अत्यधिक क्रियाशील होते हैं, और इसलिए पर्याप्त मात्रा में जैविक जीवों के लिए हानिकारक या घातक हो सकते हैं।
• फ्लोरीन सबसे अधिक क्रियाशील है और जैसे-जैसे हम समूह में नीचे जाते हैं, क्रियाशीलता कम होती जाती है।
• क्लोरीन और आयोडीन दोनों का उपयोग कीटाणुनाशक के रूप में किया जाता है।
• अपनी मौलिक अवस्था में, हैलोजन ऑक्सीकरण एजेंट होते हैं और ब्लीच में उपयोग किए जाते हैं।
•क्लोरीन अधिकांश फ़ैब्रिक ब्लीच का सक्रिय संघटक है और अधिकांश पेपर उत्पादों के उत्पादन में इसका उपयोग किया जाता है।
समूह 18 (नोबल गैस)
आवर्त सारणी के समूह 18 (पूर्व में समूह VIII) में उत्कृष्ट गैसें रासायनिक तत्व हैं। वे हीलियम, नियॉन, आर्गन, क्रिप्टन, क्सीनन और रेडॉन हैं। उन्हें कभी-कभी अक्रिय गैस या दुर्लभ गैस कहा जाता है। नोबल गैस अप्राप्य धातुओं का एक संकेत है।
आवर्त सारणी के समूह 18 के तत्व की विशेषता:
• उत्कृष्ट गैसें सभी अधातु होती हैं और इनकी विशेषता इलेक्ट्रॉनों से पूरी तरह से भरे हुए कक्ष होते हैं।
• वे कमरे के तापमान पर एकपरमाणुक गैसों के रूप में मौजूद होते हैं, यहां तक कि बड़े परमाणु द्रव्यमान वाले भी। ऐसा इसलिए है क्योंकि उनके पास आकर्षण के बहुत कमजोर अंतर-परमाणु बल हैं, और परिणामस्वरूप बहुत कम गलनांक और क्वथनांक होता हैं।
• क्रिप्टन और ज़ेनॉन एकमात्र उत्कृष्ट गैसें हैं जो किसी भी यौगिक का निर्माण करती हैं। ये तत्व ऐसा कर सकते हैं क्योंकि उनके पास एक खाली उपकक्ष में इलेक्ट्रॉनों को स्वीकार करके एक विस्तारित ऑक्टेट बनाने की क्षमता है।
न्यूलैंड का अष्टक नियम (Newlands’ law of octaves)
अष्टक का नियम, रसायन विज्ञान में, अंग्रेजी रसायनज्ञ जे.ए.आर. न्यूलैंड्स ने 1865 में कहा था कि यदि रासायनिक तत्वों को बढ़ते परमाणु भार के अनुसार व्यवस्थित किया जाए, तो समान भौतिक और रासायनिक गुणों वाले तत्व प्रत्येक सात के अंतराल के बाद आते हैं। 1864 में न्यूलैंड्स ने तत्वों को वर्गीकृत करने का प्रयास किया। संगीत में सात संगीत स्वर होते हैं। प्रत्येक आठवां समान होता है इसी तरह, न्यूलैंड ने कहा कि किसी दिए गए तत्व से शुरू होने वाला आठवां तत्व संगीत के एक सप्तक के आठवें स्वर की तरह पुनरावृत्ति करता है। इसलिए उनके इस संबंध को अष्टक का नियम कहा गया।
- न्यूलैंड के तत्वों की तालिका में लिथियम, सोडियम और पोटेशियम एक दूसरे के निकट स्थान रखते हैं।
- फ्लोरीन और क्लोरीन या ऑक्सीजन और सल्फर एक दूसरे के पास रखे गए थे।
नोट: इस वर्गीकरण ने छोटे परमाणु भार वाले तत्वों के साथ अच्छा काम किया लेकिन बड़े परमाणु भार वाले तत्वों के मामले में असफल रहा।
मेंडलीव की तालिका (Mendeleev’s table)
इसे मेंडलीव ने 1869 में प्रकाशित किया, इसने तत्वों को व्यवस्थित करने के लिए परमाणु भार का उपयोग करते हुए, अपने समय में उचित सटीकता के साथ इसे व्यवस्थित किया। मेंडलीव को लापता तत्वों के विशेषता की सटीक भविष्यवाणी करने की अनुमति देने के लिए परमाणु भार ने पर्याप्त रूप से काम किया।
परमाणु क्रमांक एक तत्व की पूर्ण परिभाषा है और आवर्त सारणी के क्रम के लिए एक तथ्यात्मक आधार देता है।
मेंडलीफ ने महसूस किया कि तत्वों के भौतिक और रासायनिक गुण उनके परमाणु द्रव्यमान से ‘आवधिक’ तरीके से संबंधित थे, और उन्हें व्यवस्थित किया ताकि समान गुणों वाले तत्वों के समूह उनकी तालिका में लंबवत स्तंभों में रहे। आधुनिक समय की आवर्त सारणी मेंडलीफ के प्रारंभिक 63 तत्वों से आगे विकसित हुई हैं।
आधुनिक आवर्त सारणी (Modern Periodic Table)
संयोजकता (VALENCY)
संयोजकता को “एक तत्व के परमाणु की अन्य तत्वों के परमाणुओं के साथ संयोजन क्षमता के रूप में परिभाषित किया जा सकता है ताकि स्थिर विन्यास प्राप्त किया जा सके (यानी अंतिम कक्ष में 8 इलेक्ट्रॉन। कुछ विशेष मामलों में यह 2 इलेक्ट्रॉन होते हैं)।
परमाणु का आकार (ATOMIC SIZE)
यह एक पृथक परमाणु के नाभिक के केंद्र से सबसे बाहरी कक्ष के इलेक्ट्रॉन के बीच की दूरी को संदर्भित करता है।
आवर्त में बाएँ से दाएँ जाने पर परमाणु त्रिज्या घटती है। यह परमाणु आवेश में वृद्धि के कारण होता है जो इलेक्ट्रॉनों को नाभिक के करीब खींचता है और परमाणु के आकार को कम करता है।
समूह में कक्षों की संख्या में वृद्धि के कारण परमाणु आकार ऊपर से नीचे की ओर बढ़ता है।
धात्विक और अधात्विक गुण (METALLIC AND NON-METALLIC PROPERTIES)
• बाएं से दाएं आवर्त में धात्विक प्रकृति घटती है जबकि अधात्विक प्रकृति बढ़ती है।
• समूह में धात्विक गुण ऊपर से नीचे की ओर बढ़ते हैं जबकि अधात्विक गुण घटते हैं।
वैद्युतऋणात्मकता (ELECTRONEGATIVITY)
एक परमाणु की साझा इलेक्ट्रॉनों की जोड़ी को अपनी ओर आकर्षित करने की सापेक्ष प्रवृत्ति को वैद्युतीयऋणात्मकता कहा जाता है। बाएं से दाएं इलेक्ट्रोनगेटिविटी का मान बढ़ता है जबकि ऊपर से नीचे इलेक्ट्रोनगेटिविटी का मान घटता है।
आयनीकरण ऊर्जा (IONIZATION ENERGY)
आयनीकरण ऊर्जा (IE) एक पृथक गैसीय परमाणु के सबसे ढीले बंधे हुए इलेक्ट्रॉन, वैलेंस इलेक्ट्रॉन, को एक धनायन बनाने के लिए आवश्यक ऊर्जा की मात्रा है।
बाएं से दाएं आवर्त में आयनन ऊर्जा का मान बढ़ता जाता है जबकि ऊपर से नीचे आयनन ऊर्जा का मान घटता है।
इलेक्ट्रान बन्धुता (ELECTRON AFFINITY)
एक परमाणु या अणु की इलेक्ट्रॉन बन्धुता को उस ऊर्जा की मात्रा के रूप में परिभाषित किया जाता है जो एक ऋणआयन बनाने के लिए गैसीय अवस्था में एक तटस्थ परमाणु या अणु में एक इलेक्ट्रॉन को जोड़ने में खर्च की जाती है। बाएं से दाएं आवर्त में इलेक्ट्रॉन बंधुता का मान बढ़ जाता है जबकि ऊपर से नीचे इलेक्ट्रॉन बंधुता का मान घट जाता है।
धात्विक गुण (METALLIC CHARACTER)
धात्विक गुण का उपयोग धात्विक तत्वों में मौजूद रासायनिक गुणों को परिभाषित करने के लिए किया जाता है। आम तौर पर, धातुएं धनायन बनाने के लिए इलेक्ट्रॉन त्यागती हैं। अधातुएँ ऋणायन बनाने के लिए इलेक्ट्रॉन ग्रहण करती हैं। उनमें ऑक्सीकरण क्षमता भी अधिक होती है इसलिए वे आसानी से ऑक्सीकृत हो जाते हैं और प्रबल अपचायक होते हैं। धातुएँ भी क्षारीय ऑक्साइड बनाती हैं; ऑक्साइड जितना अधिक क्षारीय होगा, धात्विक गुण उतना ही अधिक होगा।
जैसे-जैसे आप टेबल में बाएं से दाएं जाते हैं, धात्विक गुण कम हो जाता है, क्योंकि तत्व अपने संयोजी कोश को भरने के लिए इलेक्ट्रॉनों को आसानी से स्वीकार कर लेते हैं। इसलिए, ये तत्व ऋणायन बनाने का अधातु गुण धारण कर लेते हैं। जैसे-जैसे आप टेबल पर ऊपर जाते हैं, नाभिक के बाहरी इलेक्ट्रॉनों पर अधिक आकर्षण के कारण धात्विक गुण कम हो जाता है। यह अधिक आकर्षण परमाणुओं के लिए इलेक्ट्रॉन त्यागना और धनायन बनाना कठिन बना देता है।



 त्रिकोणमितिः स...
त्रिकोणमितिः स...
 समलम्ब चतुर्भु...
समलम्ब चतुर्भु...
 SSC और रेलवे परीक�...
SSC और रेलवे परीक�...









